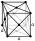Стронций
| Стронций | |
|---|---|
| Мягкий серебристо-белый металл | |
 |
|
| Название, символ, номер | Стронций / Strontium (Sr), 38 |
| Атомная масса (молярная масса) |
87,62(1) а. е. м. (г/моль) |
| Электронная конфигурация | [Kr] 5s 2 |
| Радиус атома | 215 пм |
| Ковалентный радиус | 191 пм |
| Радиус иона | (+2e) 112 пм |
| Электроотрицательность | 0,95 (шкала Полинга) |
| Электродный потенциал | −2,89 |
| Степени окисления | 2 |
| Энергия ионизации (первый электрон) |
549,0 (5,69) кДж/моль (эВ) |
| Плотность (при н. у.) | 2,54 г/см³ |
| Температура плавления | 1042 K |
| Температура кипения | 1657 K |
| Уд. теплота плавления | 9,20 кДж/моль |
| Уд. теплота испарения | 144 кДж/моль |
| Молярная теплоёмкость | 26,79 Дж/(K·моль) |
| Молярный объём | 33,7 см³/моль |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 6,080 Å |
| Температура Дебая | 147 K |
| Теплопроводность | (300 K) (35,4) Вт/(м·К) |
| Номер CAS | 7440-24-6 |
Стронций — химический элемент с атомным номером 38. Принадлежит к 2-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе II группы, или к группе IIA), находится в пятом периоде таблицы. Атомная масса элемента 87,62(1) а. е. м. . Обозначается символом Sr (от лат. Strontium ). Простое вещество стронций — мягкий, ковкий и пластичный щёлочноземельный металл серебристо-белого цвета. Обладает высокой химической активностью, на воздухе быстро реагирует с влагой и кислородом, покрываясь жёлтой оксидной плёнкой.
Содержание
История и происхождение названия
Новый элемент обнаружили в минерале стронцианите, найденном в 1764 году в свинцовом руднике близ шотландской деревни Стронти́ан (англ. Strontian , гэльск. Sròn an t-Sìthein ), давшей впоследствии название новому элементу. Присутствие в этом минерале оксида нового металла было установлено в 1787 году Уильямом Крюйкшенком и Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в 1808 году.
Нахождение в природе
В свободном виде стронций не встречается ввиду его высокой химической активности. Он входит в состав около 40 минералов. Из них наиболее важный — целестин SrSO4 (51,2 % Sr). Добывают также стронцианит SrCO3 (64,4 % Sr). Эти два минерала имеют промышленное значение. Чаще всего стронций присутствует как примесь в различных кальциевых минералах.
Среди прочих минералов стронция:
По уровню физической распространённости в земной коре стронций занимает 23-е место — его массовая доля составляет 0,014 % (в литосфере — 0,045 %). Мольная доля металла в земной коре 0,0029 %.
Стронций содержится в морской воде (8 мг/л).
Месторождения
Известны месторождения в Калифорнии, Аризоне (США); Новой Гранаде; Турции, Иране, Китае, Мексике, Канаде, Малави.
В России обнаружены, но в настоящее время не разрабатываются месторождения стронциевых руд: Синие камни (Дагестан), Мазуевское (Пермский край), Табольское (Тульская область), а также месторождения в Бурятии, Иркутской области, Красноярском крае, Якутии и на Курильских островах.
Получение
Существуют три способа получения металлического стронция:
- термическое разложение некоторых соединений;
- электролиз;
- восстановление оксида или хлорида.
Основным промышленным способом получения металлического стронция является термическое восстановление его оксида алюминием. Далее полученный стронций очищается возгонкой.
Электролитическое получение стронция электролизом расплава смеси SrCl2 и NaCl не получило широкого распространения из-за малого выхода по току и загрязнения стронция примесями.
При термическом разложении гидрида или нитрида стронция образуется мелкодисперсный стронций, склонный к лёгкому воспламенению.
Физические свойства
Стронций — мягкий серебристо-белый металл, обладает ковкостью и пластичностью, легко режется ножом.
Полиморфен — известны три его модификации. До 215 °С устойчива кубическая гранецентрированная модификация (α-Sr), между 215 и 605 °С — гексагональная (β-Sr), выше 605 °С — кубическая объёмноцентрированная модификация (γ-Sr).
Температура плавления: 768 °С, температура кипения: 1390 °С.
Химические свойства
Стронций в своих соединениях всегда проявляет степень окисления +2. По свойствам стронций близок к кальцию и барию, занимая промежуточное положение между ними.
В электрохимическом ряду напряжений стронций находится среди наиболее активных металлов (его нормальный электродный потенциал равен −2,89 В). Энергично реагирует с водой, образуя гидроксид:
Взаимодействует с кислотами, вытесняет тяжёлые металлы из их солей. С концентрированными кислотами (H2SO4, HNO3) реагирует слабо.
Металлический стронций быстро окисляется на воздухе, образуя желтоватую плёнку, в которой, помимо оксида SrO, всегда присутствуют пероксид SrO2 и нитрид Sr3N2. При нагревании на воздухе загорается, порошкообразный стронций на воздухе склонен к самовоспламенению.
Энергично реагирует с неметаллами — серой, фосфором, галогенами. Взаимодействует с водородом (выше 200 °С), азотом (выше 400 °С). Практически не реагирует со щелочами.
При высоких температурах реагирует с CO2, образуя карбид:
Легкорастворимы соли стронция с анионами Cl − , I − , NO3 − . Соли с анионами F − , SO4 2− , CO3 2− , PO4 3− малорастворимы.
Из-за высокой химической активности стронция его хранят в закрытой стеклянной посуде под слоем керосина.
Применение
Основные области применения стронция и его химических соединений — это радиоэлектронная промышленность, пиротехника, металлургия, пищевая промышленность.
Металлургия
Стронций применяется для легирования меди и некоторых её сплавов, для введения в аккумуляторные свинцовые сплавы, для десульфурации чугуна, меди и сталей.
Металлотермия
Стронций чистотой 99,99—99,999 % применяется для восстановления урана.
Магнитные материалы
Магнитотвёрдые ферриты стронция широко употребляются в качестве материалов для производства постоянных магнитов.
Пиротехника
В пиротехнике применяются карбонат, нитрат, перхлорат стронция для окрашивания пламени в карминово-красный цвет. Сплав магний-стронций обладает сильнейшими пирофорными свойствами и находит применение в пиротехнике для зажигательных и сигнальных составов.
Ядерная энергетика
Уранат стронция играет важную роль при получении водорода (стронций-уранатный цикл, Лос-Аламос, США) термохимическим способом (атомно-водородная энергетика), и, в частности, разрабатываются способы непосредственного деления ядер урана в составе ураната стронция для получения тепла при разложении воды на водород и кислород.
Высокотемпературная сверхпроводимость
Оксид стронция применяется в качестве компонента сверхпроводящих керамик.
Вакуумные электронные приборы
Оксид стронция, в составе твёрдого раствора оксидов других щёлочноземельных металлов — бария и кальция (BaO, CaO), используется в качестве активного слоя катодов косвенного накала в вакуумных электронных приборах.
Химические источники тока
Фторид стронция используется в качестве компонента твёрдотельных фторионных аккумуляторных батарей с большой энергоёмкостью и энергоплотностью.
Сплавы стронция с оловом и свинцом применяются для отливки токоотводов аккумуляторных батарей. Сплавы стронций-кадмий — для анодов гальванических элементов.
Медицина
Изотоп с атомной массой 89, имеющий период полураспада 50,55 суток, применяется (в виде хлорида) в качестве противоопухолевого средства.
Биологическая роль
Влияние на организм человека
Не следует путать действие на организм человека природного стронция (не радиоактивного, малотоксичного и более того, широко используемого для лечения остеопороза) и радиоактивных изотопов стронция.
Стронций природный — составная часть микроорганизмов, растений и животных. Стронций является аналогом кальция, поэтому он наиболее эффективно откладывается в костной ткани. В мягких тканях задерживается менее 1 %. Стронций с большой скоростью накапливается в организме детей до четырёхлетнего возраста, когда идёт активное формирование костной ткани. Обмен стронция изменяется при некоторых заболеваниях органов пищеварения и сердечно-сосудистой системы.
- вода (предельно допустимая концентрация стронция в воде в РФ — 8 мг/л, а в США — 4 мг/л)
- пища (томаты, свёкла, укроп, петрушка, редька, редис, лук, капуста, ячмень, рожь, пшеница)
- интратрахеальное поступление
- через кожу (накожное)
- ингаляционное (через лёгкие)
- люди, работа которых связана со стронцием (в медицине радиоактивный стронций используют в качестве аппликаторов при лечении кожных и глазных болезней.
Основные области применения:
- природного стронция — радиоэлектронная промышленность, пиротехника, металлургия, металлотермия, пищевая промышленность, производство магнитных материалов;
- радиоактивного — производство атомных электрических батарей, атомно-водородная энергетика, радиоизотопные термоэлектрические генераторы и другое).
Влияние нерадиоактивного стронция проявляется крайне редко и только при воздействии других факторов (дефицит кальция и витамина D, неполноценное питание, нарушения соотношения микроэлементов таких, как барий, молибден, селен и другие). Тогда он может вызывать у детей «стронциевый рахит» и «уровскую болезнь» — поражение и деформацию суставов, задержку роста и другие нарушения.
Радиоактивный стронций практически всегда негативно воздействует на организм человека. Откладываясь в костях, он облучает костную ткань и костный мозг, что увеличивает риск заболевания злокачественными опухолями костей, а при поступлении большого количества может вызвать лучевую болезнь.
Изотопы
В природе стронций встречается в виде смеси четырёх стабильных изотопов 84 Sr (0,56(2) %), 86 Sr (9,86(20) %), 87 Sr (7,00(20) %), 88 Sr (82,58(35) %). Проценты указаны по числу атомов. Известны также радиоактивные изотопы стронция с массовым числом от 73 до 105. Лёгкие изотопы (до 85 Sr включительно, а также изомер 87m Sr) испытывают электронный захват, распадаясь в соответствующие изотопы рубидия. Тяжёлые изотопы, начиная с 89 Sr, испытывают β − -распад, переходя в соответствующие изотопы иттрия. Наиболее долгоживущим и важным в практическом плане среди радиоактивных изотопов стронция является 90 Sr.
Стронций-90
Изотоп стронция 90 Sr является радиоактивным с периодом полураспада 28,78 года . 90 Sr претерпевает β − -распад, переходя в радиоактивный 90 Y (период полураспада 64 часа), который, в свою очередь, распадается в стабильный цирконий-90. Полный распад стронция-90, попавшего в окружающую среду, произойдёт лишь через несколько сотен лет.
90 Sr образуется при ядерных взрывах и внутри ядерного реактора во время его работы. Образование стронция-90 при этом происходит как непосредственно в результате деления ядер урана и плутония, так и в результате бета-распада короткоживущих ядер с массовым числом A = 90 (в цепочке 90 Se → 90 Br → 90 Kr → 90 Rb → 90 Sr ), образующихся при делении.
Применяется в производстве радиоизотопных источников энергии в виде титаната стронция (плотность 4,8 г/см³ , а энерговыделение — около 0,54 Вт/см³ ).
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs |
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu,
Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2,
W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, Au
Источник статьи: http://chem.ru/stroncij.html
Стронций
Стронций / Strontium (Sr), 38
Стро́нций — элемент главной подгруппы второй группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 38. Обозначается символом Sr (лат. Strontium ). Простое вещество стронций (CAS-номер: 7440-24-6) — мягкий, ковкий и пластичный щёлочноземельный металл серебристо-белого цвета. Обладает высокой химической активностью, на воздухе быстро реагирует с влагой и кислородом, покрываясь жёлтой оксидной плёнкой.
Содержание
История и происхождение названия
Новый элемент обнаружили в минерале стронцианите, найденном в 1764 году в свинцовом руднике близ шотландской деревни Строншиан, давшей впоследствии название новому элементу. Присутствие в этом минерале оксида нового металла было установлено в 1787 году Уильямом Крюйкшенком и Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в 1808 году.
Нахождение в природе
В свободном виде стронций не встречается. Он входит в состав около 40 минералов. Из них наиболее важный — целестин SrSO4 (51,2 % Sr). Добывают также стронцианит SrCO3 (64,4 % Sr). Эти два минерала имеют промышленное значение. Чаще всего стронций присутствует как примесь в различных кальциевых минералах.
Среди прочих минералов стронция:
По уровню физической распространённости в земной коре стронций занимает 23-е место — его массовая доля составляет 0,014 % (в литосфере — 0,045 %). Мольная доля металла в земной коре 0,0029 %. Стронций содержится в морской воде (8 мг/л) [3] .
В природе стронций встречается в виде смеси 4 стабильных изотопов 84 Sr (0,56 %), 86 Sr (9,86 %), 87 Sr (7,02 %), 88 Sr (82,56 %).
Месторождения
Известны месторождения стронция в Калифорнии, Аризоне (США); России и других странах [4] [5] .
Получение
Существуют 3 способа получения металлического стронция:
- термическое разложение некоторых соединений
- электролиз
- восстановление оксида или хлорида
Основным промышленным способом получения металлического стронция является термическое восстановление его оксида алюминием. Далее полученный стронций очищается возгонкой.
Электролитическое получение стронция электролизом расплава смеси SrCl2 и NaCl не получило широкого распространения из-за малого выхода по току и загрязнения стронция примесями.
При термическом разложении гидрида или нитрида стронция образуется мелкодисперсный стронций, склонный к легкому воспламенению.
Физические свойства
Стронций — мягкий серебристо-белый металл, обладает ковкостью и пластичностью, легко режется ножом.
Полиморфен — известны три его модификации. До 215 о С устойчива кубическая гранецентрированная модификация (α-Sr), между 215 и 605 о С — гексагональная (β-Sr), выше 605 о С — кубическая объемно-центрированная модификация (γ-Sr).
Температура плавления — 768 о С, Температура кипения — 1390 о С.
Химические свойства
Стронций в своих соединениях всегда проявляет валентность +2. По свойствам стронций близок к кальцию и барию, занимая промежуточное положение между ними.
В электрохимическом ряду напряжений стронций находится среди наиболее активных металлов (его нормальный электродный потенциал равен −2,89 В). Энергично реагирует с водой, образуя гидроксид:
Взаимодействует с кислотами, вытесняет тяжёлые металлы из их солей. С концентрированными кислотами (H2SO4, HNO3) реагирует слабо.
Металлический стронций быстро окисляется на воздухе, образуя желтоватую плёнку, в которой помимо оксида SrO всегда присутствуют пероксид SrO2 и нитрид Sr3N2. При нагревании на воздухе загорается, порошкообразный стронций на воздухе склонен к самовоспламенению.
Энергично реагирует с неметаллами — серой, фосфором, галогенами. Взаимодействует с водородом (выше 200 о С), азотом (выше 400 о С). Практически не реагирует с щелочами.
При высоких температурах реагирует с CO2, образуя карбид:
Легкорастворимы соли стронция с анионами Cl − , I − , NO3 − . Соли с анионами F − , SO4 2− , CO3 2− , PO4 3− малорастворимы.
Применение
Основные области применения стронция и его химических соединений — это радиоэлектронная промышленность, пиротехника, металлургия, пищевая промышленность.
Металлургия
Стронций применяется для легирования меди и некоторых её сплавов, для введения в аккумуляторные свинцовые сплавы, для десульфурации чугуна, меди и сталей.
Металлотермия
Стронций чистотой 99,99—99,999 % применяется для восстановления урана.
Магнитные материалы
Магнитотвёрдые ферриты стронция широко употребляются в качестве материалов для производства постоянных магнитов.
Пиротехника
В пиротехнике применяются карбонат, нитрат, перхлорат стронция для окрашивания пламени в карминово-красный цвет. Сплав магний-стронций обладает сильнейшими пирофорными свойствами и находит применение в пиротехнике для зажигательных и сигнальных составов.
Атомноводородная энергетика
Уранат стронция играет важную роль при получении водорода (стронций-уранатный цикл, Лос-Аламос, США) термохимическим способом (атомно-водородная энергетика), и в частности разрабатываются способы непосредственного деления ядер урана в составе ураната стронция для получения тепла при разложении воды на водород и кислород.
Высокотемпературная сверхпроводимость
Оксид стронция применяется в качестве компонента сверхпроводящих керамик.
Вакуумные электронные приборы
Оксид стронция, в составе твёрдого раствора оксидов других щёлочноземельных металлов — бария и кальция (BaO, CaO), используется в качестве активного слоя катодов косвенного накала в вакуумных электронных приборах.
Химические источники тока
Фторид стронция используется в качестве компонента твердотельных фторионных аккумуляторных батарей с большой энергоемкостью и энергоплотностью.
Сплавы стронция с оловом и свинцом применяются для отливки токоотводов аккумуляторных батарей. Сплавы стронций-кадмий для анодов гальванических элементов.
Медицина
Изотоп с атомной массой 89, имеющий период полураспада 50,55 суток, применяется (в виде хлорида) в качестве противоопухолевого средства [6] [7] .
Биологическая роль
Влияние на организм человека
Не следует путать действие на организм человека природного (нерадиоактивного, малотоксичного и более того, широко используемого для лечения остеопороза) и радиоактивных изотопов стронция [8] .
Стронций природный — составная часть микроорганизмов, растений и животных. Стронций является аналогом кальция, поэтому он наиболее эффективно откладывается в костной ткани. В мягких тканях задерживается менее 1 %. Стронций с большой скоростью накапливается в организме детей до четырёхлетнего возраста, когда идет активное формирование костной ткани. Обмен стронция изменяется при некоторых заболеваниях органов пищеварения и сердечно-сосудистой системы.
- вода (предельно допустимая концентрация стронция в воде в РФ — 8 мг/л, а в США — 4 мг/л [8] )
- пища (томаты, свёкла, укроп, петрушка, редька, редис, лук, капуста, ячмень, рожь, пшеница)
- интратрахеальное поступление
- через кожу (накожное)
- ингаляционное (через лёгкие)
- люди, работа которых связана со стронцием (в медицине радиоактивный стронций используют в качестве аппликаторов при лечении кожных и глазных болезней. Основные области применения природного стронция — это радиоэлектронная промышленность, пиротехника, металлургия, металлотермия, пищевая промышленность, пр-во магнитных материалов, радиоактивного — пр-во атомных электрических батарей. атомно-водородная энергетика, радиоизотопные термоэлектрические генераторы и др.)
Влияние нерадиоактивного стронция проявляется крайне редко и только при воздействии других факторов (дефицит кальция и витамина Д, неполноценное питание, нарушения соотношения микроэлементов таких как барий, молибден, селен и др.). Тогда он может вызывать у детей «стронциевый рахит» и «уровскую болезнь» — поражение и деформация суставов, задержка роста и другие нарушения.
Радиоактивный стронций практически всегда негативно воздействует на организм человека. Откладываясь в костной ткани, он облучает костную ткань и костный мозг, что увеличивает риск заболевания раком костного мозга, а при поступлении большого количества может вызвать лучевую болезнь.
Изотопы
Стронций-90
Изотоп стронция 90 Sr является радиоактивным с периодом полураспада 28.9 лет. 90 Sr претерпевает β-распад, переходя в радиоактивный 90 Y (период полураспада 64 ч.) Полный распад стронция-90, попавшего в окружающую среду, произойдет лишь через несколько сотен лет. 90 Sr образуется при ядерных взрывах и внутри ядерного реактора во время его работы.
Применяется в производстве радиоизотопных источников тока в виде титаната стронция (плотность 4,8 г/см³, а энерговыделение около 0,54 Вт/см³).
Источник статьи: http://dic.academic.ru/dic.nsf/ruwiki/7782
Стронций
Большая советская энциклопедия. — М.: Советская энциклопедия . 1969—1978 .
Полезное
Смотреть что такое “Стронций” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
Стронций — хим. элемент II гр. периодической системы, порядковый номер 38, ат. в. 87, 63; состоит из 4 стабильных изотопов. Средний изотопный состав обычного С. следующий: Sr84 0,56%, Si86 9,86%, Sr87 7,02%, Sr88 82,56%. Один из изотопов С. Sr87… … Геологическая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
СТРОНЦИЙ — (Strontium), Sr, хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно земельный металл. Природный С. смесь стабильных 84Sr, 86Sr 88Sr, в к рой преобладает 88Sr (82,58%), а меньше всего 84Sr (0,56%).… … Физическая энциклопедия
Источник статьи: http://dic.academic.ru/dic.nsf/bse/136529/%D0%A1%D1%82%D1%80%D0%BE%D0%BD%D1%86%D0%B8%D0%B9
Стронций: способы получения и химические свойства
Стронций Sr — это щелочноземельный металл. Светло-желтый, ковкий. Реакционноспособный; Сильный восстановитель.
Относительная молекулярная масса Mr = 87,62; относительная плотность для твердого и жидкого состояния d = 2,63; tпл = 768º C; tкип = 1390º C.
Способ получения
1. В результате реакции между оксидом стронция и алюминием при 1200º С образуются стронций и алюминат стронция :
4SrO + 2Al = 3Sr + Sr(AlO2)2
2. Хлорид стронция взаимодействует с алюминием при 600 — 700º С образуя стронций и хлорид стронция:
3SrCl2 + 2Al = 3Sr + 2AlCl3
3. В результате электролиза жидкого хлорида стронция образуется стронций и хлор:
4. Сульфид стронция разлагается при температуре выше 2000º С с образованием стронция и серы:
Качественная реакция
Окрашивает пламя газовой горелки в ярко-красный цвет.
Химические свойства
1. Стронций — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами :
1.1. Стронций взаимодействует с азотом при 450 — 500º С образуя нитрид стронция:
1.2. Стронций сгорает в кислороде (воздухе) при выше 250º С с образованием оксида стронция:
2Sr + O2 = 2SrO
1.3. Стронций активно реагирует при 200 — 400º С с хлором . При этом образуется хлорид стронция :
1.4. С водородом стронций реагирует при температуре 200 — 500º C с образованием гидрида стронция:
1.5. Стронций вступает в реакцию при 500º С с углеродом и образует карбид стронция:
Sr + 2C = SrC2
2. Стронций активно взаимодействует со сложными веществами:
2.1. Стронций реагирует при комнатной температуре с водой . Взаимодействие стронция с водой приводит к образованию гидроксида стронция и газа водорода:
2.2. Стронций взаимодействует с кислотами:
2.2.1. Стронций реагирует с разбавленной соляной кислотой, при этом образуются хлорид стронция и водород :
Sr + 2HCl = SrCl2 + H2 ↑
2.2.2. Реагируя с разбавленной азотной кислотой стронций образует нитрат стронция, оксид азота (I) и воду:
а если стронций будет взаимодействовать с очень разбавленной азотной кислотой , то на выходе будет образовываться нитрат стронция, нитрат аммония и вода:
2.3. Стронций вступает в реакцию с газом аммиаком при 600 — 650º С. В результате данной реакции образуется нитрид стронция.
в результате взаимодействия жидкого аммиака и стронция в присутствии катализатора Pt происходит образование амида стронция и воды
Источник статьи: http://chemege.ru/stroncij/
СТРОНЦИЙ
(Strontium), Sr,- хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно-земельный металл. Природный С.- смесь стабильных 84 Sr, 86 Sr- 88 Sr, в к-рой преобладает 88 Sr (82,58%), а меньше всего 84 Sr (0,56%). Конфигурация внеш. электронной оболочки 5s 2 . Энергии последоват. ионизации равны соответственно 5,695, 11,030, 42,884, 56,3, 71,6 эВ. Радиус атома С. 0,215 нм, радиус иона Sr 2+ 0,120 нм. Значение электроотрицательности 0,99.
В свободном виде – мягкий золотисто-жёлтый металл. При темп-pax от комнатной до 248 °С устойчив a-Sr с ку-бич. гранецентриров. решёткой (параметр а= 0,6085 нм), при темп-рах 248-557 °С – b-Sr с гексагональной решёткой (параметры а =0,432 нм и с= 0,706 нм), от 557 °С до t пл = 768 °С – g-Sr с кубич. объёмноцентриров. решёткой (параметр a= 0,485 нм). Плотность a-Sr 2,630 кг/дм 3 , t кип = 1390 °С, теплоёмкость с р = 26,81 Дж/(моль•К), теплота плавления 8,38 кДж/моль, теплота сублимации 151,7 кДж/моль, теплота кипения 134 кДж/моль. Уд. элек-трич. сопротивление 0,20 мкОм•м (при О °С), термич. коэф. электрич. сопротивления 5,2•10 -3 K -1 (при 0-200 °С). Магн. восприимчивость 1,05•10 -9 . Ср. термич. коэф. линейного расширения 2,3•10 -5 К -1 . Модуль нормальной упругости 16,0 ГПа, модуль сдвига 6,08 ГПа, модуль объёмного сжатия 12,2 ГПа.
Химически высокоактивен, реагирует с кислородом и азотом воздуха, степень окисления в соединениях +2. По хим. свойствам аналогичен кальцию и барию.
Металлич. С. используют в качестве газопоглотителя в эл.-вакуумных приборах, его добавляют в алюминиевые и др. спец. сплавы. Фторид С.- люминофор, лазерный и оптич. материал. Добавка оксида С. (SrO) в стёкла улучшает их радиац. стойкость. Соли С. [нитрат С. Sr(NO 3 ) 2 и др.] применяют в пиротехнике для окрашивания пламени. При делении ядер U в ядерных реакторах и при взрывах ядерного оружия образуются значит. кол-ва b-радиоактивных нуклидов С.: 89 Sr(T 1/2 = 50,5 сут) и 90 Sr(T 1/2 = 29,12 года), к-рые представляют большую опасность для окружающей среды (особенно 90 Sr), т. к. длит. время находятся в поверхностном слое Земли и обладают
высокой миграционной способностью. 90 Sr накапливается в костных тканях живых организмов, замещая Са, что ведёт к хрупкости костей и др. вредным воздействиям на организм, поэтому актуальна проблема очистки от него сточных вод АЭС и др. С. С. Бердоносов.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия . Главный редактор А. М. Прохоров . 1988 .
Полезное
Смотреть что такое “СТРОНЦИЙ” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
Стронций — хим. элемент II гр. периодической системы, порядковый номер 38, ат. в. 87, 63; состоит из 4 стабильных изотопов. Средний изотопный состав обычного С. следующий: Sr84 0,56%, Si86 9,86%, Sr87 7,02%, Sr88 82,56%. Один из изотопов С. Sr87… … Геологическая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
Источник статьи: http://dic.academic.ru/dic.nsf/enc_physics/4829/%D0%A1%D0%A2%D0%A0%D0%9E%D0%9D%D0%A6%D0%98%D0%99
Стронций
Геологический словарь: в 2-х томах. — М.: Недра . Под редакцией К. Н. Паффенгольца и др. . 1978 .
Литература : Бурков B. B., Подпорина E. K., Cтронций, M., 1962; Фop Г., Пауэлл Дж., Изотопы стронция в геологии, пер. c англ., M., 1974; Aналитическая химия стронция, M., 1978.
C. Ф. Kарпенко.
Горная энциклопедия. — М.: Советская энциклопедия . Под редакцией Е. А. Козловского . 1984—1991 .
Полезное
Смотреть что такое “Стронций” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
СТРОНЦИЙ — (Strontium), Sr, хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно земельный металл. Природный С. смесь стабильных 84Sr, 86Sr 88Sr, в к рой преобладает 88Sr (82,58%), а меньше всего 84Sr (0,56%).… … Физическая энциклопедия
Источник статьи: http://dic.academic.ru/dic.nsf/enc_geolog/4867/%D0%A1%D1%82%D1%80%D0%BE%D0%BD%D1%86%D0%B8%D0%B9
стронций
Энциклопедический словарь . 2009 .
Полезное
Смотреть что такое “стронций” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
Стронций — хим. элемент II гр. периодической системы, порядковый номер 38, ат. в. 87, 63; состоит из 4 стабильных изотопов. Средний изотопный состав обычного С. следующий: Sr84 0,56%, Si86 9,86%, Sr87 7,02%, Sr88 82,56%. Один из изотопов С. Sr87… … Геологическая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
СТРОНЦИЙ — (Strontium), Sr, хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно земельный металл. Природный С. смесь стабильных 84Sr, 86Sr 88Sr, в к рой преобладает 88Sr (82,58%), а меньше всего 84Sr (0,56%).… … Физическая энциклопедия
Источник статьи: http://dic.academic.ru/dic.nsf/es/54858/%D1%81%D1%82%D1%80%D0%BE%D0%BD%D1%86%D0%B8%D0%B9
СТРОНЦИЙ
(от назв. деревни Строншиан, Strontian, в Шотландии, близ к-рой был обнаружен; лат. Strontium) Sr, хим. элемент II гр. периодич. системы, ат. н. 38, ат. м. 87,62; относится к щелочноземельным элементам. Природный С. состоит из четырех стабильных изотопов: 88 Sr(82,56%), 86 Sr(9,86%), 87 Sr(7,02%) и 84 Sr(0,56%). Поперечное сечение захвата тепловых нейтронов для прир. смеси изотопов 1,21
Химическая энциклопедия. — М.: Советская энциклопедия . Под ред. И. Л. Кнунянца . 1988 .
Смотреть что такое “СТРОНЦИЙ” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
Стронций — хим. элемент II гр. периодической системы, порядковый номер 38, ат. в. 87, 63; состоит из 4 стабильных изотопов. Средний изотопный состав обычного С. следующий: Sr84 0,56%, Si86 9,86%, Sr87 7,02%, Sr88 82,56%. Один из изотопов С. Sr87… … Геологическая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
СТРОНЦИЙ — (Strontium), Sr, хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно земельный металл. Природный С. смесь стабильных 84Sr, 86Sr 88Sr, в к рой преобладает 88Sr (82,58%), а меньше всего 84Sr (0,56%).… … Физическая энциклопедия
Источник статьи: http://dic.academic.ru/dic.nsf/enc_chemistry/4289/%D0%A1%D0%A2%D0%A0%D0%9E%D0%9D%D0%A6%D0%98%D0%99
Стронций
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб.: Брокгауз-Ефрон . 1890—1907 .
Полезное
Смотреть что такое “Стронций” в других словарях:
СТРОНЦИЙ — (ново лат.). Легкий металл желтого цвета, названный так по имени деревни в Шотландии, в окрестностях которой открыт впервые; в соединении с углекислотою образует минерал стронцианит. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
Стронций-90 — Таблица нуклидов Общие сведения Название, символ Стронций 90, 90Sr Альтернативные названия Радиостронций Нейтронов 52 Протонов 38 Свойства нуклида Атомная масса 8 … Википедия
СТРОНЦИЙ — хим. элемент, символ Sr (лат. Strontium), ат. н. 38, ат. м. 87,62; относится к щёлочноземельным металлам, имеет серебристо белый цвет, плотность 2630 кг/м3, tпл = 768 °С. Химически очень активен, поэтому в чистом виде применяется мало. Используют … Большая политехническая энциклопедия
Стронций — хим. элемент II гр. периодической системы, порядковый номер 38, ат. в. 87, 63; состоит из 4 стабильных изотопов. Средний изотопный состав обычного С. следующий: Sr84 0,56%, Si86 9,86%, Sr87 7,02%, Sr88 82,56%. Один из изотопов С. Sr87… … Геологическая энциклопедия
стронций — целестин Словарь русских синонимов. стронций сущ., кол во синонимов: 5 • иностранец (23) • метал … Словарь синонимов
СТРОНЦИЙ — (Strontium), Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62; мягкий щелочноземельный металл. В результате ядерных испытаний, аварий на АЭС и с радиоактивными отходами в окружающую среду попадает… … Современная энциклопедия
СТРОНЦИЙ — (лат. Strontium) Sr, химический элемент II группы периодической системы, атомный номер 38, атомная масса 87,62, относится к щелочноземельным металлам. Назван по минералу стронцианиту, найденному около д. Строншиан (Strontian) в Шотландии.… … Большой Энциклопедический словарь
СТРОНЦИЙ — СТРОНЦИЙ, стронция, мн. нет, муж. (лат. strontium) (хим.). Очень легкий металл желтоватого цвета. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СТРОНЦИЙ — СТРОНЦИЙ, я, муж. Химический элемент, лёгкий серебристо белый металл. Радиоактивный изотоп стронция. | прил. стронциевый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
СТРОНЦИЙ — муж. один из химически открытых металлов, схожий с барием; стронциан, нная, новая земля, окись стронция. Стронцит, цианит, углекислый стронциан. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
СТРОНЦИЙ — (Strontium), Sr, хим. элемент II группы периодич. системы элементов, ат. номер 38, ат. масса 87,62, щёлочно земельный металл. Природный С. смесь стабильных 84Sr, 86Sr 88Sr, в к рой преобладает 88Sr (82,58%), а меньше всего 84Sr (0,56%).… … Физическая энциклопедия
Источник статьи: http://dic.academic.ru/dic.nsf/brokgauz_efron/97815/%D0%A1%D1%82%D1%80%D0%BE%D0%BD%D1%86%D0%B8%D0%B9
Стронций
| Стронций | ||||||||||||||||||||||||||||||||||||||
 Стронций хранится в атмосфере аргона. |
||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||
| Положение в периодической таблице | ||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Символ | Sr | |||||||||||||||||||||||||||||||||||||
| Фамилия | Стронций | |||||||||||||||||||||||||||||||||||||
| Атомный номер | 38 | |||||||||||||||||||||||||||||||||||||
| Группа | 2 | |||||||||||||||||||||||||||||||||||||
| Период | 5- й период | |||||||||||||||||||||||||||||||||||||
| Блокировать | Блок s | |||||||||||||||||||||||||||||||||||||
| Семейство элементов | Щелочноземельный металл | |||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Kr ] 5 с 2 | |||||||||||||||||||||||||||||||||||||
| Электроны по уровню энергии | 2, 8, 18, 8, 2 | |||||||||||||||||||||||||||||||||||||
| Атомарные свойства элемента | ||||||||||||||||||||||||||||||||||||||
| Атомная масса | 87,62 ± 0,01 ед. | |||||||||||||||||||||||||||||||||||||
| Атомный радиус (расч.) | 219 вечера | |||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 195 ± 10 часов вечера | |||||||||||||||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 249 вечера | |||||||||||||||||||||||||||||||||||||
| Состояние окисления | 2 | |||||||||||||||||||||||||||||||||||||
| Электроотрицательность ( Полинг ) | 0,95 | |||||||||||||||||||||||||||||||||||||
| Окись | Сильная база | |||||||||||||||||||||||||||||||||||||
| Энергии ионизации | ||||||||||||||||||||||||||||||||||||||
| 1 re : 5,69485 эВ | 2 e : 11,0301 эВ | |||||||||||||||||||||||||||||||||||||
| 3 e : 42,89 эВ | 4 th : 57 эВ | |||||||||||||||||||||||||||||||||||||
| 5 e : 71,6 эВ | 6 e : 90,8 эВ | |||||||||||||||||||||||||||||||||||||
| 7 th : 106 эВ | 8 e : 122,3 эВ | |||||||||||||||||||||||||||||||||||||
| 9 e : 162 эВ | 10 th : 177 эВ | |||||||||||||||||||||||||||||||||||||
| 11 e : 324,1 эВ | ||||||||||||||||||||||||||||||||||||||
| Самые стабильные изотопы | ||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||
| Простые физические свойства тела | ||||||||||||||||||||||||||||||||||||||
| Обычное состояние | Твердый ( парамагнитный ) | |||||||||||||||||||||||||||||||||||||
| Объемная масса | 2,64 г · см -3 | |||||||||||||||||||||||||||||||||||||
| Кристаллическая система | Гранецентрированная кубическая | |||||||||||||||||||||||||||||||||||||
| Твердость | 1.5 | |||||||||||||||||||||||||||||||||||||
| Цвет | Металлик Серебристо-Белый | |||||||||||||||||||||||||||||||||||||
| Точка слияния | 777 ° С | |||||||||||||||||||||||||||||||||||||
| Точка кипения | 1382 ° С | |||||||||||||||||||||||||||||||||||||
| Энергия термоядерного синтеза | 8,3 кДж · моль -1 | |||||||||||||||||||||||||||||||||||||
| Энергия парообразования | 144 кДж · моль -1 | |||||||||||||||||||||||||||||||||||||
| Молярный объем | 33,94 × 10 -6 м 3 · моль -1 | |||||||||||||||||||||||||||||||||||||
| Давление газа | 246 Па в 768,85 ° C | |||||||||||||||||||||||||||||||||||||
| Массовое тепло | 300 Дж · кг -1 · К -1 | |||||||||||||||||||||||||||||||||||||
| Электрическая проводимость | 7,62 х 10 6 См · м -1 | |||||||||||||||||||||||||||||||||||||
| Теплопроводность | 35,3 Вт · м -1 · К -1 | |||||||||||||||||||||||||||||||||||||
| Разные | ||||||||||||||||||||||||||||||||||||||
| Н о CAS | 7440-24-6 | |||||||||||||||||||||||||||||||||||||
| N о ИК | 100 028 303 | |||||||||||||||||||||||||||||||||||||
| N о ЕС | 231-133-4 | |||||||||||||||||||||||||||||||||||||
| Меры предосторожности | ||||||||||||||||||||||||||||||||||||||
| SGH | ||||||||||||||||||||||||||||||||||||||