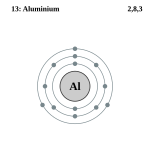
Склонение слова «Алюминий»
Склонение слова по падежам: именительный, родительный, дательный, винительный, творительный, предложный. В множественном и единственном числе. Удобный поиск склонений для слов, более 83451 слов в нашей базе. Посмотрите обучающий видео урок как правильно склонять слова.
Единственное число
| Падеж | Вопрос | Слово |
|---|---|---|
| именительный | Кто, что? | алюминий |
| родительный | Кого, чего? | алюминия |
| дательный | Кому, чему? | алюминию |
| винительный | Кого, что? | алюминий |
| творительный | Кем, чем? | алюминием |
| предложный | О ком, о чём? | алюминии |
Множественное число
| Падеж | Вопрос | Слово |
|---|---|---|
| именительный | Кто, что? | алюминии |
| родительный | Кого, чего? | алюминиев |
| дательный | Кому, чему? | алюминиям |
| винительный | Кого, что? | алюминии |
| творительный | Кем, чем? | алюминиями |
| предложный | О ком, о чём? | алюминиях |
Важно знать о склонении слов
Склонение существительных
Изменение имён существительных по падежам характеризуется изменением их окончаний, которые называются падежными формами. Всего в русском языке существует шесть падежей, каждый из которых имеет свой вспомогательный вопрос.
Для того, чтобы определить падеж имени существительного, нужно попробовать задать к нему один из вспомогательных вопросов.
Также существуют несклоняемые имена существительные, т.е. те, которые имеют во всех падежах одну и ту же форму. К несклоняемым относятся как имена нарицательные (например, “кофе” или “какао”), так и имена собственные (например, “Гёте”).
Как правило, несклоняемыми существительными оказываются слова, заимствованные из иностранных языков. Они могут относиться ко всем трем родам.
Склонение имен числительных
Склонение числительных не имеет единого образца, оно представлено несколькими типами:
- Числительное один склоняется как прилагательное в единственном числе: один — одного (новый — нового).
- Числительные от пяти до десяти и числительные на -дцать и -десят склоняются как существительные 3-склонения. У числительных на -десят два окончания, так как изменяются обе части: пятидесяти, пятьюдесятью.
- Числительные сорок, девяносто, сто, полтора и полтораста, изменяясь по падежам, имеют только две формы: именительный и винительный падежи — сорок, девяносто, сто, полтора, полтораста; родительный, дательный, творительный, предложный падежи — сорока, девяноста, ста, полутора, полутораста.
- Числительные от двухсот до четырехсот и от пятисот до девятисот склоняются по особому типу.
- Собирательные числительные также склоняются по особому типу. Числительные оба, обе имеют два разных варианта склонения.
- Простые порядковые числительные склоняются как прилагательные: первый (новый) — первого (нового). У сложных порядковых числительных только одно окончание. У составных порядковых числительных изменяется только последняя часть.
- У дробных числительных при склонении изменяются обе части.
Склонение прилагательных
Склонение прилагательных – это изменение их по родам, падежам и числам.
Однако не все прилагательные изменяются и по родам, и по числам, и по падежам. Краткие прилагательные не изменяются по падежам, а прилагательные в форме простой сравнительной степени вообще не склоняются.
Для того, чтобы правильно склонять имена прилагательные, нужно знать их падежные вопросы в обоих числах.
Важно понимать, что окончание прилагательного можно проверить окончанием вопроса.
Видеоурок. Изменение личных местоимений по падежам
Источник статьи: http://sklonenie-slova.ru/alyuminiy
Алюминий или аллюминий?
Русский язык богат словами, которые так и просятся быть написанными неправильно: О вместо А, одну согласную вместо двух и наоборот. Именно таким словом выступает существительное алюминий, в котором многие пишущие совершают одну и ту же ошибку. Так как же пишется алюминий: с одной Л или с двумя?
Правописание слова
Русский язык заимствовал немало слов из разных языков, в частности, из греческого и латинского. Одним из таких слов и является слово алюминий. Обратимся к происхождению этого слова. Согласно «Объяснению 25 000 иностранных слов, вошедших в употребление в русском языке» А. Михельсона, этимология восходит к латинскому alumen, то есть «квасцы», из которых впервые алюминий и добыли. Неизвестное вещество назвали aluminium, а мы знаем его под именем алюминий.
Впрочем, неудивительно, что рука то и дело стремится добавить к этому существительному ещё одну Л: у нас действительно множество иностранных, но давно привычных нам слов, которые пишутся с удвоенной сонорной согласной – М, Л или Н – в корне:
Поэтому часто хочется написать так же и другие заимствованные слова типа «волейбол», «галерея», «гуманизм». При этом, как правило, заимствование из других языков вынуждает нас писать слова близкими к оригиналу, такова языковая традиция. Поэтому и аЛюминий мы пишем с одной Л в корне. Никакой проверочной формы этого существительного не существует, его нужно просто запомнить!
Тем не менее, можно прибегнуть к мнемонике. Например, использовать шуточный приём, старый анекдот:
– Сегодня будем грузить люминь! – Товарищ прапорщик, не люминь, а алюминий… – А самые умные будут грузить чугуний!
Так как написать слово «люминь» с двумя Л довольно проблематично, поэтому запомнить правописание нужного нам слова оказывается совсем несложно!
Примеры предложений
- Однако несмотря на легкость, алюминий – очень прочный металл.
- Алюминиевые кастрюли моя бабушка чистила обычным песком.
- — Не люблю эту алюминиевую сковородку, — ворчала мама. – Так как она слишком быстро нагревается.
- Недорогая и долговечная, алюминиевая посуда быстро завоевала популярность у покупателей.
Ошибочное написание
Неправильным считается написание данного слово следующим образом писать: «аллюминий», «олюминий», «оллюминий».
Синонимы
Синонимами к этому существительному могут быть только эпитеты к металлу: «легкий, крылатый, серебристый металл», «металл для самолетов».
Заключение
Итак, чтобы запомнить правописание аЛюминия, никакого правила не существует. Это слово можно либо просто запомнить, либо воспользоваться мнемоническим приемом, либо же просто заглянуть в орфографический словарь.
Источник статьи: http://correctno.ru/orfografiya/alyuminiy_ili_allyuminiy
Как пишется слово «алюминий» или «аллюминий»?
Слово «алюминий» пишется с одной буквой «л» в корне.
Часто возникает вопрос, как правильно пишется слово «алюминий» или «аллюминий» в русском языке? Чтобы выбрать правильный вариант написания этого существительного с одной буквой или с двойными согласными в корне обратимся к его происхождению.
Правописание слова «алюминий»
Интересующее нас слово является заимствованным в русском языке. Оно начинается с гласной «а». Что интересно, почти все лексемы с начальной гласной «а» являются заимствованными в русском языке. Следы рассматриваемого слова приведут нас в латинский язык, где исходное aluminis буквально значит «квасцы». Как видим, в языке-источнике в слове пишется одна буква «л». Рассматриваемое существительное единственного числа мужского рода сохраняет такое же написание в русском языке.
Алюминий всем знаком!
Нам исправно служит он.
Втрое он полегче стали.
Прочен в сплавах и притом
Смело входит в каждый дом.
Провода висят у вас? Это раз!
Если есть сковорода — это два!
Самолет и теплоход,
Трактор или вездеход —
Для любых таких конструкций
Алюминий подойдёт!
Аналогичное написание прослеживается в однокоренном прилагательном «алюминиевый», существительном «алюмель» (сплав никеля с алюминием), «алюминаты» и в сложных словах-терминах «алюминотермия», «алюмосиликаты».
Буквой «л» передается на письме звонкий сонорный звук [л’], который произносится с известной долей голоса по сравнению с другими согласными, которые звучат довольно коротко, с шумом и имеют пары по признаку звонкости/глухости :
Видимо, поэтому при произношении слова «алюминий» звучит длинный согласный «л», который хочется на письме удвоить.
Укажем ряд заимствованных слов, в корне которых, несмотря на произношение, пишется также одна буква «л» :
- а л огизм, ба л юстрада, га л ерея, га л антерея, га л ета, кава л ерия;
- ка л ория, ка л орийный, ка л орийность, ко л ичество, ко л орит.
Написание перечисленных слов запомним или в случае затруднения справимся о них в орфографическом словаре.
Источник статьи: http://russkiiyazyk.ru/orfografiya/pravopisanie/alyuminiy-ili-allyuminiy.html
«АЛюминий» или «аЛЛюминий» − как правильно пишется?
Правописание русского языка непростое. Где-то пишется двойная согласная, где-то происходит чередование гласных. Как пишется алюминий – в этом надо разобраться.
Значение и разбор слова
В процессе эволюции языка в нем появилось много заимствованных слов. Алюминий − одно из них. Это химический элемент белого цвета, лёгкий. Хорошо формуется. Атомный номер 13.
Устойчивый к коррозии. Применяется в приборостроении, в авиации, строительстве. В природе в чистом виде не существует.
Слово произошло от латинского alumen. Оно значит квасцы, из которых впервые добыли метал. Вариант aluminium появился в начале 20 века и сохранился до наших дней.
8 букв и 8 звуков. Несмотря на то, что в слове 4 слога, вариантов переноса 3. Первый слог не может отрываться от лексемы, потому что состоит из 1 буквы.
Все согласные сонорные, мягкие, звонкие, непарные. Чтобы разобрать «алюминий» по составу, надо выделить окончание. Для этого необходимо изменить формы лексемы (алюминию, алюминием, алюминия). Й − окончание, алюмини − основа.
В последнюю входят приставка, суффикс, корень. Префикса в слове нет. Для выделения корня надо подобрать однокоренные слова: алюминат, алюминиевый, алюминий. Общая часть − алюмин.
Морфема, заключенная между корнем и окончанием, называется суффиксом. В лексеме это «и».
«Алюминий» − это нарицательное, неодушевленное существительное 2-го скл. и мужского рода. Стоит в единственном числе, именит. падеже. Точно определить последнюю категорию можно только в контенте. Лексема не употребляется во множественном числе.
Разбор правила орфографии
Как правильно пишется алюминий или аллюминий. Варианты написания слов, заимствованных из других языков, воспроизводятся близко к оригиналу. Таковы правила грамматики. Название металла пришло от латинского aluminium. В родном языке лексема пишется с одной «л». Это же написание сохранилось в русском.
В некоторых заимствованных словах вместо 2-х согласных, которые пишутся в оригинале, в русском осталась только 1. Gallery − галерея office − офис. Но нет ни одного случая, чтобы фонемы добавлялись.
Для слов с иностранным происхождением правил правописания не существует. Их надо запомнить.
Примеры предложений
В походе алюминиевые кастрюли мы чистили песком.
Алюминий используют для производства консервных банок.
Источник статьи: http://nauka.club/russkiy-yazyk/orfografiya/alyuminiy-ili-allyuminiy-kak-pravilno-pishetsya.html
«Алюминий» или «аллюминий», как правильно?
Слово «алюминий» пишется с одной буквой «л» в корне.
Часто возникает вопрос, как правильно пишется слово «алюминий» или «аллюминий»? Чтобы выбрать правильный вариант написания этого существительного с одной буквой или с двойными согласными в корне обратимся к его происхождению.
Правописание слова «алюминий»
Интересующее нас слово является заимствованным в русском языке. Оно начинается с гласной «а». Что интересно, почти все лексемы с начальной гласной «а» являются заимствованными в русском языке. Следы рассматриваемого слова приведут нас в латинский язык, где исходное aluminis значит «квасцы». Как видим, в языке-источнике в слове пишется одна буква «л». В таком виде данное существительное пришло в русский язык и сохраняет это написание.
Слово «алюминий» пишется с одной буквой «л» в корне.
Алюминий всем знаком!
Нам исправно служит он.
Втрое он полегче стали.
Прочен в сплавах и притом
Смело входит в каждый дом.
Провода висят у вас? Это раз!
Если есть сковорода — это два!
Самолет и теплоход,
Трактор или вездеход —
Для любых таких конструкций
Алюминий подойдёт!
Такое же написание прослеживается в однокоренном прилагательном «алюминиевый», существительном «алюмель» (сплав никеля с алюминием), «алюминаты» и в сложных словах-терминах «алюминотермия», «алюмосиликаты».
Буквой «л» передается на письме звонкий сонорный звук [л’], который произносится с известной долей голоса по сравнению с другими согласными, которые произносятся довольно коротко, с шумом и имеют пары по признаку звонкости/глухости :
Видимо, поэтому при произношении слова «алюминий» звучит длинный согласный «л», который хочется на письме удвоить.
Укажем ряд заимствованных слов, в корне которых, несмотря на произношение, пишется также одна буква «л» :
- а л огизм, ба л юстрада, га л ерея, га л антерея, га л ета, кава л ерия;
- ка л ория, ка л орийный, ка л орийность, ко л ичество, ко л орит.
Написание перечисленных слов запомним или в случае затруднения справимся о них в орфографическом словаре.
Как правильно пишется слово «аллея» поинтересуемся в статье, где рассматривается, почему в его корне пишутся двойные согласные «л».
Источник статьи: http://sprint-olympic.ru/uroki/russkij-jazyk-uroki/kak-pravilno-pishetsja/42375-aljuminij-ili-alljuminij-kak-pravilno.html
«Алюминиевый» как правильно пишется?
Как пишется слово?
Если вы хотите узнать, как правильно пишется какое-либо слово, необходимо узнать какой частью речи является это слово. Далее найти правило русского языка, которое определяет правописание. Давайте разбираться.
Слово «алюминиевый» от существительного «алюминий». Прилагательное «алюминиевый» пишется так же, как в в латинском варианте (alumen) с одной буквой «л». Написание необходим запомнить.
Правильно пишется:
«АЛЮМИНИЕВЫЙ»
Прочие варианты написания слова
Алюминиевый — прилагательное мужского рода единственного числа
| Ед. число | Мн. число | ||||
|---|---|---|---|---|---|
| Муж. род | Жен. род | Средний род | |||
| Им. | норм. | алюминиевый | алюминиевая | алюминиевое | алюминиевые |
| прев. | — | — | — | — | |
| Род. | норм. | алюминиевого | алюминиевой | алюминиевого | алюминиевых |
| прев. | — | — | — | — | |
| Дат. | норм. | алюминиевому | алюминиевой | алюминиевому | алюминиевым |
| прев. | — | — | — | — | |
| Винит. одуш. |
норм. | алюминиевого | алюминиевую | алюминиевое | алюминиевых |
| прев. | — | — | — | — | |
| Винит. неодуш. |
норм. | алюминиевый | алюминиевую | алюминиевое | алюминиевые |
| прев. | — | — | — | — | |
| Тв. | норм. | алюминиевым | алюминиевой , алюминиевою |
алюминиевым | алюминиевыми |
| прев. | — | — | — | — | |
| Пред. | норм. | алюминиевом | алюминиевой | алюминиевом | алюминиевых |
| прев. | — | — | — | — | |
| Кр. прил. | алюминиев | алюминиева | алюминиево | алюминиевы | |
| Сравнит. ст. | алюминиевее , алюминиевей , поалюминиевее , поалюминиевей |
||||
Например
Это был обыкновенный алюминиевый стаканчик для бритья.
Она взяла из коробки большую алюминиевую кружку и пошла к озеру.
Источник статьи: http://pravopisanie.com/kak-pishetsya-aluminievii/
«Алюминий» или «аллюминий», как правильно?
Слово «алюминий» пишется с одной буквой «л» в корне.
Часто возникает вопрос, как правильно пишется слово «алюминий» или «аллюминий»? Чтобы выбрать правильный вариант написания этого существительного с одной буквой или с двойными согласными в корне обратимся к его происхождению.
Правописание слова «алюминий»
Интересующее нас слово является заимствованным в русском языке. Оно начинается с гласной «а». Что интересно, почти все лексемы с начальной гласной «а» являются заимствованными в русском языке. Следы рассматриваемого слова приведут нас в латинский язык, где исходное aluminis значит «квасцы». Как видим, в языке-источнике в слове пишется одна буква «л». В таком виде данное существительное пришло в русский язык и сохраняет это написание.
Слово «алюминий» пишется с одной буквой «л» в корне.
Алюминий всем знаком!
Нам исправно служит он.
Втрое он полегче стали.
Прочен в сплавах и притом
Смело входит в каждый дом.
Провода висят у вас? Это раз!
Если есть сковорода — это два!
Самолет и теплоход,
Трактор или вездеход —
Для любых таких конструкций
Алюминий подойдёт!
Такое же написание прослеживается в однокоренном прилагательном «алюминиевый», существительном «алюмель» (сплав никеля с алюминием), «алюминаты» и в сложных словах-терминах «алюминотермия», «алюмосиликаты».
Буквой «л» передается на письме звонкий сонорный звук [л’], который произносится с известной долей голоса по сравнению с другими согласными, которые произносятся довольно коротко, с шумом и имеют пары по признаку звонкости/глухости :
Видимо, поэтому при произношении слова «алюминий» звучит длинный согласный «л», который хочется на письме удвоить.
Укажем ряд заимствованных слов, в корне которых, несмотря на произношение, пишется также одна буква «л» :
- а л огизм, ба л юстрада, га л ерея, га л антерея, га л ета, кава л ерия;
- ка л ория, ка л орийный, ка л орийность, ко л ичество, ко л орит.
Написание перечисленных слов запомним или в случае затруднения справимся о них в орфографическом словаре.
Как правильно пишется слово «аллея» поинтересуемся в статье, где рассматривается, почему в его корне пишутся двойные согласные «л».
Источник статьи: http://sprint-olympic.ru/uroki/russkij-jazyk-uroki/kak-pravilno-pishetsja/42375-aljuminij-ili-alljuminij-kak-pravilno.html
Основные свойства алюминия: области применения
Вопросы, рассмотренные в материале:
- Как был открыт алюминий и каковы его основные свойства
- Основные физические свойства алюминия
- Основные химические свойства алюминия
- Как применяют основные свойства алюминия
- Как используют основные свойства алюминия в строительстве
Основные свойства алюминия делают этот материал по-настоящему универсальным и ценным. Его используют во всех видах промышленного производства, в сельском хозяйстве, в быту, в коммерции. Обладает огромным количеством преимуществ по отношению к стали и другим видам металла.
Самые популярные сферы применения алюминия – изготовление металлоконструкций и металлообработка. О том, какие свойства металла и где конкретно они нашли свое применение, читайте далее.
Как был открыт алюминий и каковы его основные свойства
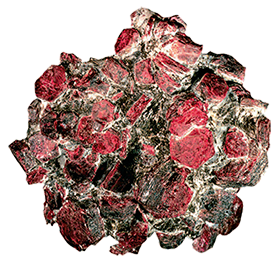
Алюминий представляет собой парамагнитный металл, достаточно легкий, имеющий серебристый цвет. Он хорошо поддается механической обработке и литью, просто формуется. В земной коре этот элемент третий по распространенности, впереди только кислород и кремний. Наши недра содержат целых 8 % данного металла, что значительно больше золота, количество которого составляет не более пяти миллионных долей процента.
Алюминий активно используется в большинстве сфер производства. Его сплавы применяются для изготовления бытовой техники, транспорта, в машиностроении и электротехнике. Капитальное строительство также не может обойтись без него.
Он чрезвычайно распространен в земной коре, являясь первым из металлов и третьим химическим элементом (первое место у кислорода, второе – у кремния). Доля алюминия в наших недрах – 8,8 %. Металл является частью большого количества горных пород и минералов, основной из которых – алюмосиликат.
В виде соединений алюминий находится в базальтах, полевых шпатах, гранитах, глине и пр. Однако в основном его получают из бокситов, которые достаточно редко встречаются в виде месторождений. В России такие залежи есть только на Урале и в Сибири. В промышленных масштабах алюминий можно также добывать из нефелинов и алунитов.
Рекомендуем статьи по металлообработке
Ткани животных и растений содержат алюминий в виде микроэлемента. Некоторые организмы, например, моллюски и плауны, являются его концентраторами, накапливая в своих органах.
Человечеству с давних времен знакомо соединение алюминия под названием алюмокалиевые квасцы. Применялось оно в процессе выделки кожи, в качестве средства, которое, набухая, связывает различные компоненты смеси. Во второй половине XVIII в. ученые открыли оксид алюминия. А вот вещество в чистом виде получили значительно позже.
Впервые это удалось Ч. К. Эрстеду, который выделил алюминий из хлорида. Проводя опыт, он обрабатывал соли калия амальгамой, в результате чего выделился порошок серого цвета, признанный всеми чистым алюминием.
В дальнейшем, исследуя металл, ученые определили его химические свойства, проявляющиеся в высокой способности к восстановлению и активности. Именно поэтому с алюминием долгое время не работали.
Но уже в 1854 г. французский ученый Девиль, применив электролиз расплава, сумел получить металл в слитках. Данный метод используется и сейчас. В промышленных масштабах алюминий стали производить в начале XX в., когда предприятия смогли получить доступ к большому количеству электроэнергии.
Сегодня алюминий является одним из самых используемых в производстве бытовой техники и строительстве металлом.
Основные физические свойства алюминия
Основные характеристики алюминия – высокая электро- и теплопроводность, пластичность, устойчивость к холоду и коррозии. Его можно обрабатывать посредством прокатки, ковки, штамповки, волочения. Алюминий прекрасно поддается сварке.
Примеси, присутствующие в металле в различных количествах, значительно ухудшают механические, технологические и физико-химические свойства чистого алюминия. Основными из них являются титан, кремний, железо, медь и цинк.
По степени очистки алюминий разделяют на технический металл и высокой чистоты. На практике различия данных типов – в стойкости к коррозии в различной среде. Стоимость напрямую зависит от чистоты алюминия. Технический металл подходит для производства проката, различных сплавов, кабельно-проводниковых изделий. Чистый используют для специальных целей.
Алюминий обладает высокой электропроводностью, уступая только золоту, серебру, меди. Однако сочетание данного показателя с малой плотностью позволяет использовать его при производстве кабельно-проводниковых изделий наравне с медью. Электропроводность металла может увеличиваться при длительном отжиге или ухудшаться при нагартовке.
Увеличивая чистоту алюминия, производители повышают его теплопроводность. Снизить данное свойство способны примеси меди, марганца и магния. Более высокую теплопроводность имеют исключительно медь и серебро. Именно благодаря данному свойству данный металл используют для производства радиаторов охлаждения и теплообменников.
Удельная теплоемкость алюминия, как и температура его плавления, достаточно высока. Данные показатели значительно превышают аналогичные значения большей части металлов. С повышением чистоты металла увеличивается и его способность отражать от поверхности световые лучи. Алюминий хорошо поддается полировке и прекрасно анодируется.
Металл близок по свойствам к кислороду, его поверхность на воздухе быстро затягивается пленкой из оксида алюминия – тонкой и прочной. Обладая антикоррозионными свойствами, она защищает металл от образования ржавчины и предупреждает дальнейшее окисление. Алюминий не взаимодействует с азотной кислотой (концентрированной и разбавленной) и органическими кислотами, он стоек к воздействию пресной, соленой воды.
Эти особенности алюминия придают ему устойчивость к коррозии, что и используется людьми. Именно поэтому его особенно широко применяют в строительстве. Интерес к нему увеличивается еще и по причине его легкости в сочетании с прочностью и мягкостью. Такие характеристики есть далеко не у всякого вещества.
Помимо вышеуказанных, алюминий имеет еще несколько интересных физических свойств:
- Ковкость и пластичность – алюминий стал материалом изготовления прочной и легкой тонкой фольги, а также проволоки.
- Плавление происходит при температуре +660 °С.
- Температура кипения +2 450 °С.
- Плотность – 2,7 г/см³.
- Наличие объемной гранецентрированной металлической кристаллической решетки.
- Тип связи – металлический.
Области использования алюминия определяются его химическими и физическими свойствами. Характеристики металла, рассмотренные выше, применяются в бытовых целях. Основные свойства алюминия, как прочного, особо легкого, антикоррозийного материала, используются в судо- и авиастроении. Именно поэтому важно их знать.
Основные химические свойства алюминия
С химической точки зрения алюминий является чрезвычайно сильным восстановителем, имеющим способность в чистом виде быть высоко активным веществом. Основное условие – убрать оксидную пленку.
Алюминий способен вступать в реакции с:
- щелочными соединениями;
- кислотами;
- серой;
- галогенами.
Алюминий не взаимодействует в обычных условиях с водой. Йод – единственный из галогенов, с которым у металла происходит реакция без нагревания. Для взаимодействия с прочими требуется увеличение температуры.
Рассмотрим несколько примеров, показывающих химические свойства данного металла. Это уравнения, иллюстрирующие взаимодействие с:
Основным свойством алюминия считается его способность восстанавливать иные вещества из их соединений.
Реакции его взаимодействия с оксидами иных металлов хорошо показывают все восстановительные свойства вещества. Алюминий прекрасно выделяет металлы из различных соединений. Примером может служить: Cr2O3 + AL = AL2O3 + Cr.
Металлургическая промышленность активно использует эту способность алюминия. Методика получения веществ, которая основывается на данной реакции, называется алюминотермия. Химическая индустрия использует алюминий чаще всего для получения иных металлов.
Как применяют основные свойства алюминия
Алюминий в чистом виде имеет слабые механические свойства. Именно поэтому наиболее часто применяют его сплавы.
Таких сплавов достаточно много, вот основные из них:
- алюминий с марганцем;
- дюралюминий;
- алюминий с магнием;
- алюминий с медью;
- авиаль;
- силумины.
В основе этих сплавов лежит алюминий, отличаются они исключительно добавками. Последние же делают материал прочным, легким в обработке, более стойким к износу, коррозии.
Есть несколько основных областей применения алюминия (чистого или в виде сплава). Из металла изготавливают:
- фольгу и проволоку для бытового использования;
- посуду;
- морские и речные суда;
- самолеты;
- реакторы;
- космические аппараты;
- архитектурные и строительные элементы и конструкции.
Алюминий является одним из самых важных металлов наравне с железом и его сплавами. Эти два элемента таблицы Менделеева наиболее широко применяются человеком в своей деятельности.
Как используют основные свойства алюминия в строительстве
Строительство – одна из основных отраслей-потребителей алюминия. 25 % всего вырабатываемого металла используется именно в ней. Современный облик мегаполисов был бы невозможен без использования алюминия. Он дает возможность создавать функциональные и красивые здания, стремящиеся ввысь. Небоскребы офисных центров имеют фасады из стекла, закрепленные на прочных, легких рамах из алюминия.
Современные торговые, развлекательные и выставочные центры в основе своей имеют каркас из алюминия. Конструкции из данного металла используются для возведения бассейнов, стадионов и других спортивных строений. Алюминий – один из самых востребованных у архитекторов, строителей, дизайнеров металлов. Почему? Давайте разберемся.
Алюминий – прочный и легкий металл, не поддающийся коррозии, имеющий долгий срок службы и совершенно нетоксичный. Он легко поддается обработке, сварке, паянию, его просто сверлить, распиливать, связывать и соединять шурупами. Этот металл способен принять любую форму посредством экструзии. Алюминий поможет воплотить самый смелый замысел архитектора. Из него изготавливаются конструкции, которые невозможно сделать из иных материалов: пластика, дерева или стали.
За прошлый век алюминий прошел путь от металла, редко используемого в строительстве из-за дороговизны и недостаточных объемов производства, до наиболее часто применяемого. 1920-е годы стали переломными. Благодаря электролизной технологии значительно снизилась стоимость его производства – в 5 раз. Алюминий стали применять в производстве стеновых панелей и водостоков, декоративных элементов, а не только для сводов и отделки крыш.
Empire State Building – первый небоскреб, при возведении которого широко применялся алюминий. Он был построен в 1931 году и оставался самым высоким в мире до 1970 г.
Алюминий активно использовался в конструкциях этого здания. В интерьере его также применяли достаточно широко. Фреска, расположенная на стенах и полке лобби, являющаяся визитной карточкой сооружения, сделана из алюминия и золота в 23 карата.
80 лет – таков минимальный срок эксплуатации конструкций из алюминия. Применение этого металла не ограничено климатическими условиями, его свойства остаются прежними при температурах от -80 °С и до +300 °C. Пожары редко могут разрушить алюминиевые сооружения. Низкие же температуры, наоборот, увеличивают его прочность.
Примером может служить алюминиевый сайдинг. Отражающее покрытие в виде фольги и теплоизоляция создают вместе с ним прекрасную защиту от холода, которая в 4 раза более эффективна, чем облицовка кирпичом толщиной 10 см или камнем толщиной 20 см. Именно поэтому алюминий все чаще можно встретить при строительстве объектов в условиях холодного климата: в РФ – на Северном Урале, в Якутии и Сибири.
Но еще более важным качеством алюминия является его легкость. При одинаковой жесткости пластина из алюминия в два раза легче стальной. И все благодаря низкому удельному весу. Если посчитать, то выйдет, что вес алюминиевой конструкции при равной несущей способности в два, а иногда и в три раза ниже массы стальной и в семь раз ниже железобетонной.
В настоящее время алюминий используют для строительства небоскребов и иных высоких строений. Металл делает здание значительно легче, что удешевляет постройку за счет меньшей глубины фундамента. Ведь чем больший вес имеют сооружения, тем фундамент должен быть глубже. Разводные мосты, выполненные из алюминия, также имеют небольшой вес, что облегчает работу механизмов, противовесы для таких конструкций должны быть минимальными. Данный металл вообще дает возможность архитекторам не ограничивать фантазию. Да и работать с таким легким материалом значительно проще, быстрее и удобнее.
Источник статьи: http://vt-metall.ru/articles/424-osnovnye-svojstva-alyuminiya/
Об алюминии
Алюминий – серебристо-белый металл, 13-й элемент периодической таблицы Менделеева. Невероятно, но факт: алюминий – самый распространенный металл на Земле, на него приходится более 8% всей массы земной коры, и это третий по распространенности химический элемент на нашей планете после кислорода и кремния.
При этом алюминий не встречается в природе в чистом виде из-за своей высокой химической активности. Вот почему мы узнали о нем относительно недавно. Формально алюминий был получен лишь в 1824 году, и прошло еще полвека, прежде чем началось его промышленное производство.
Чаще всего в природе алюминий встречается в составе квасцов. Это минералы, объединяющие в себе две соли серной кислоты: одну на основе щелочного металла (лития, натрия, калия, рубидия или цезия), а другую – на основе металла третьей группы таблицы Менделеева, преимущественно алюминия.
Квасцы и сегодня применяют при очистке воды, в кулинарии, медицине, косметологии, в химической и других отраслях промышленности. Кстати, свое имя алюминий получил как раз благодаря квасцам, которые на латыни назывались alumen.
Но каким бы распространенным ни был алюминий, его открытие стало возможным только, когда в распоряжении ученых появился новый инструмент, позволяющий расщеплять сложные вещества на простые, – электрический ток.
И в 1824 году с помощью процесса электролиза датский физик Ханс Кристиан Эрстед получил алюминий. Он был загрязнен примесями калия и ртути, задействованных в химических реакциях, однако это был первый случай получения алюминия.
Используя электролиз, алюминий производят и в наши дни.
Сырьем для производства алюминия сегодня служит еще одна распространенная в природе алюминиевая руда – бокситы. Это глинистая горная порода, состоящая из разнообразных модификаций гидроксида алюминия с примесью оксидов железа, кремния, титана, серы, галлия, хрома, ванадия, карбонатных солей кальция, железа и магния – чуть ли не половины таблицы Менделеева. В среднем из 4-5 тонн бокситов производится 1 тонна алюминия.
Из бокситов получают глинозем. Это оксид алюминия Al2O3, который имеет форму белого порошка и из которого путем электролиза на алюминиевых заводах производят металл.
Производство алюминия требует огромного количества электроэнергии. Для производства одной тонны металла необходимо около 15 МВт*ч энергии – столько потребляет 100-квартирный дом в течение целого месяца.Поэтому разумнее всего строить алюминиевые заводы поблизости от мощных и возобновляемых источников энергии. Самое оптимальное решение – гидроэлектростанции, представляющие самый мощный из всех видов «зеленой энергетики».
Легкий
Прочный
Пластичный
Нет коррозии
Алюминий легко обрабатывается давлением, причем как в горячем, так и в холодном состоянии. Он поддается прокатке, волочению, штамповке. Алюминий не горит, не требует специальной окраски и не токсичен в отличие от пластика.
Очень высока ковкость алюминия: из него можно изготовить листы толщиной всего 4 микрона и тончайшую проволоку. А сверхтонкая алюминиевая фольга втрое тоньше человеческого волоса. Кроме того, по сравнению с другими металлами и материалами он более экономичен.
Высокая способность к образованию соединений с различными химическими элементами породила множество сплавов алюминия. Даже незначительная доля примесей существенно меняет характеристики металла и открывает новые сферы для его применения. Например, сочетание алюминия с кремнием и магнием в повседневной жизни можно встретить буквально на дороге – в форме литых колесных дисков, двигателей, в элементах шасси и других частей современного автомобиля. А если добавить в алюминиевый сплав цинк, то, возможно, вы сейчас держите его в руках, ведь именно этот сплав используется при производстве корпусов мобильных телефонов и планшетов. Тем временем ученые продолжают изобретать новые и новые алюминиевые сплавы.
Сегодня существование строительной, автомобильной, авиационной, космической, электротехнической, энергетической, пищевой и других отраслей промышленности невозможно без алюминия. Более того, именно этот металл стал символом прогресса – все новейшие электронные устройства, средства передвижения изготавливаются из алюминия.
Алюминий против меди
Казалось бы, вышеперечисленный набор характеристик уже сам по себе достаточен для того, чтобы алюминий стал металлом приоритетного выбора в индустрии, однако есть еще одна, не менее значимая характеристика. Использование алюминия может быть бесконечно: этот металл и сплавы из него можно неоднократно переплавлять без утраты механических характеристик. Ученые подсчитали, что 1 кг собранных и сданных в переплавку алюминиевых банок позволяет сэкономить 8 кг боксита, 4 кг различных фторидов и 14 кВт/ч электроэнергии.
Около 75% алюминия, выпущенного за все время существования отрасли, используется до сих пор.
В статье использованы фотоматериалы © Shutterstock и © Rusal.
Источник статьи: http://aluminiumleader.ru/about_aluminium/what_is_aluminum/
Алюминий
| люминий | |
|---|---|
| Атомный номер | 13 |
| Внешний вид простого вещества |  мягкий лёгкий мягкий лёгкий металл серебристо-белого цвета |
| Свойства атома | |
| Атомная масса (молярная масса) |
26,981539 а. е. м. (г/моль) |
| Радиус атома | 143 пм |
| Энергия ионизации (первый электрон) |
577,2(5,98) кДж/моль (эВ) |
| Электронная конфигурация | [Ne] 3s 2 3p 1 |
| Химические свойства | |
| Ковалентный радиус | 118 пм |
| Радиус иона | 51 (+3e) пм |
| Электроотрицательность (по Полингу) |
1,61 |
| Электродный потенциал | -1,66 в |
| Степени окисления | 3 |
| Термодинамические свойства простого вещества | |
| Плотность | 2,6989 г/см³ |
| Молярная теплоёмкость | 24,35 [1] Дж/(K·моль) |
| Теплопроводность | 237 Вт/(м·K) |
| Температура плавления | 933,5 K |
| Теплота плавления | 10,75 кДж/моль |
| Температура кипения | 2792 K |
| Теплота испарения | 284,1 кДж/моль |
| Молярный объём | 10,0 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 4,050 Å |
| Отношение c/a | — |
| Температура Дебая | 394 K |
Алюми́ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементов Д. И. Менделеева, атомный номер 13. Обозначается символом Al ( Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости (после кислорода и кремния) химический элемент в земной коре.
Простое вещество алюминий (CAS-номер: 7429-90-5) — лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.
По некоторым биологическим исследованиям поступление алюминия в организм человека было сочтено фактором в развитии болезни Альцгеймера, но эти исследования были позже раскритикованы и вывод о связи одного с другим опровергался.
История
Впервые алюминий был получен Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути.
Получение
Современный метод получения был разработан независимо американцем Чарльзом Холлом и французом Полем Эру. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке.
Для производства 1 т алюминия чернового требуется 1,920 т глинозёма, 0,065 т криолита, 0,035 т фторида алюминия, 0,600 т анодной массы и 17 тыс. кВт·ч электроэнергии постоянного тока.
Физические свойства
Металл серебристо-белого цвета, лёгкий, плотность — 2,7 г/см³, температура плавления у технического алюминия — 658 °C, у алюминия высокой чистоты — 660 °C, удельная теплота плавления — 390 кДж/кг, температура кипения — 2500 °C, удельная теплота испарения — 10,53 МДж/кг, временное сопротивление литого алюминия — 10-12 кг/мм², деформируемого — 18-25 кг/мм², сплавов — 38-42 кг/мм².
Твёрдость по Бринеллю — 24-32 кгс/мм², высокая пластичность: у технического — 35 %, у чистого — 50 %, прокатывается в тонкий лист и даже фольгу.
Алюминий обладает высокой электропроводностью и теплопроводностью, 65 % от электропроводности меди, обладает высокой светоотражательной способностью.
Алюминий образует сплавы почти со всеми металлами.
Нахождение в природе
Природный алюминий состоит практически полностью из единственного стабильного изотопа 27 Al со следами 26 Al, радиоактивного изотопа с периодом полураспада 720 тыс. лет, образующегося в атмосфере при бомбардировке ядер аргона протонами космических лучей.
По распространённости в природе занимает 1-е среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Процент содержания алюминия в земной коре по данным различных исследователей составляет от 7,45 до 8,14 % от массы земной коры.
В природе алюминий встречается только в соединениях (минералах). Некоторые из них:
В природных водах алюминий содержится в виде малотоксичных химических соединений, например, фторида алюминия. Вид катиона или аниона зависит, в первую очередь, от кислотности водной среды. Концентрации алюминия в поверхностных водных объектах России колеблются от 0,001 до 10 мг/л.
Химические свойства
При нормальных условиях алюминий покрыт тонкой и прочной оксидной плёнкой и потому не реагирует с классическими окислителями: с H2O (t°);O2, HNO3 (без нагревания). Благодаря этому алюминий практически не подвержен коррозии и потому широко востребован современной индустрией. Однако при разрушении оксидной плёнки (например, при контакте с растворами солей аммония NH4 + , горячими щелочами или в результате амальгамирования), алюминий выступает как активный металл-восстановитель.
Легко реагирует с простыми веществами:
Сульфид и карбид алюминия полностью гидролизуются:
- с водой (после удаления защитной оксидной пленки, например, амальгамированием или растворами горячей щёлочи): 2Al + 6H2O = 2Al(OH)3 + 3H2
- со щелочами (с образованием тетрагидроксоалюминатов и других алюминатов): 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 2(NaOH•H2O) + 2Al = 2NaAlO2 + 3H2
- Легко растворяется в соляной и разбавленной серной кислотах: 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 3H2SO4(разб) = Al2(SO4)3 + 3H2
- При нагревании растворяется в кислотах — окислителях, образующих растворимые соли алюминия: 2Al + 6H2SO4(конц) = Al2(SO4)3 + 3SO2 + 6H2O Al + 6HNO3(конц) = Al(NO3)3 + 3NO2 + 3H2O
- восстанавливает металлы из их оксидов (алюминотермия): 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + Cr2O3 = Al2O3 + 2Cr
Производство
Одна красивая, но, вероятно, неправдоподобная легенда из «Historia naturalis« гласит, что однажды к римскому императору Тиберию (42 год до н. э. — 37 год н. э.) пришёл ювелир с металлической, небьющейся обеденной тарелкой, изготовленной, якобы из глинозёма — Al2O3. Тарелка была очень светлой и блестела, как серебро. По всем признакам она должна быть алюминиевой. При этом ювелир утверждал, что только он и боги знают, как получить этот металл из глины. Тиберий, опасаясь, что металл из легкодоступной глины может обесценить золото и серебро, приказал, на всякий случай, отрубить человеку голову. Очевидно, данная легенда весьма сомнительна, так как самородный алюминий в природе не встречается в силу своей высокой активности и во времена Римской империи не могло быть технических средств, которые позволили бы извлечь алюминий из глинозёма.
Лишь почти через 2000 лет — в 1825 году, датский физик Ханс Христиан Эрстед получил несколько миллиграммов металлического алюминия, а в 1827 году Фридрих Вёлер смог выделить крупинки алюминия, которые, однако, на воздухе немедленно покрывались тончайшей пленкой оксида алюминия.
До конца XIX века алюминий в промышленных масштабах не производился.
Только в 1854 году Анри Сент-Клер Девиль изобрёл первый способ промышленного производства алюминия, основанный на вытеснении алюминия металлическим натрием из двойного хлорида натрия и алюминия NaCl·AlCl3. В 1855 году был получен первый слиток металла массой 6—8 кг. За 36 лет применения, с 1855 по 1890 год, способом Сент-Клер Девиля было получено 200 тонн металлического алюминия. В 1856 году он же получил алюминий электролизом расплава хлорида натрия-алюминия.
В 1885 году, основываясь на технологии, предложенной русским ученым Николаем Бекетовым, был построен завод по производству алюминия в немецком городе Гмелингеме. Технология Бекетова мало чем отличалась от способа Девиля, но была проще и заключалась во взаимодействии между криолитом (Na3AlF6) и магнием. За пять лет на этом заводе было получено около 58 т алюминия — более четверти всего мирового производства металла химическим путем в период с 1854 по 1890 год.
Метод, изобретённый почти одновременно Чарльзом Холлом во Франции и Полем Эру в США в 1886 году и основанный на получении алюминия электролизом глинозема, растворённого в расплавленном криолите, положил начало современному способу производства алюминия. С тех пор, в связи с усовершенствованием электротехники, производство алюминия совершенствовалось. Заметный вклад в развитие производства глинозема внесли русские ученые К. И. Байер, Д. А. Пеняков, А. Н. Кузнецов, Е. И. Жуковский, А. А. Яковкин и др.
Первый алюминиевый завод в России был построен в 1932 году в Волхове. Металлургическая промышленность СССР в 1939 году производила 47,7 тыс.тонн алюминия, ещё 2,2 тыс.тонн импортировалось.
Вторая мировая война значительно стимулировала производство алюминия. Так, в 1939 году общемировое его производство, без учёта СССР, составляло 620 тыс. т, но уже к 1943 году выросло до 1,9 млн т.
К 1956 году в мире производилось 3,4 млн т первичного алюминия, в 1965 году — 5,4 млн т, в 1980 году — 16,1 млн т, в 1990 году — 18 млн т.
В 2007 году в мире было произведено 38 млн т первичного алюминимя, а в 2008 — 39,7 млн т. Лидерами производства являлись: Китай (в 2007 году произвёл 12,60 млн т, а в 2008 — 13,50 млн т), Россия (3,96/4,20), Канада (3,09/3,10), США (2,55/2,64), Австралия (1,96/1,96), Бразилия (1,66/1,66), Индия (1,22/1,30), Норвегия (1,30/1,10), ОАЭ (0,89/0,92), Бахрейн (0,87/0,87), ЮАР (0,90/0,85), Исландия (0,40/0,79), Германия (0,55/0,59), Венесуэла (0,61/0,55), Мозамбик (0,56/055), Таджикистан (0,42/0,42).
В России фактическим монополистом по производству алюминия является ОАО «Русский алюминий», на который приходится около 13 % мирового рынка алюминия и 16 % глинозёма.
Мировые запасы бокситов практически безграничны, то есть несоизмеримы с динамикой спроса. Существующие мощности могут производить до 44,3 млн т первичного алюминия в год. Следует также учитывать, что в будущем некоторые из применений алюминия могут быть переориентированы на использование, например, композитных материалов.
Применение
Широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной плёнкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки.
Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния – сплав дюралюминий.
Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 2 раза дешевле. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Меньшую электропроводность алюминия (37 1/ом) по сравнению с медью (63 1/ом) компенсируют увеличением сечения алюминиевых проводников. Недостатком алюминия как электротехнического материала является прочная оксидная плёнка, затрудняющая спаивание.
- Благодаря комплексу свойств широко распространён в тепловом оборудовании.
- Алюминий и его сплавы сохраняют прочность при сверхнизких температурах. Благодаря этому он широко используется в криогенной технике.
- Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью напыления делает алюминий идеальным материалом для изготовления зеркал.
- В производстве строительных материалов как газообразующий агент.
- Алитированием придают коррозионную и окалиностойкость стальным и другим сплавам, например клапанам поршневых ДВС, лопаткам турбин, нефтяным платформам, теплообменной аппаратуре, а также заменяют цинкование.
- Сульфид алюминия используется для производства сероводорода.
- Идут исследования по разработке пенистого алюминия как особо прочного и лёгкого материала.
В качестве восстановителя
- Как компонент термита, смесей для алюмотермии
- Алюминий применяют для восстановления редких металлов из их оксидов или галогенидов.
Сплавы на основе алюминия
В качестве конструкционного материала обычно используют не чистый алюминий, а разные сплавы на его основе.
— Алюминиево-магниевые сплавы обладают высокой коррозионной стойкостью и хорошо свариваются; из них делают, например, корпуса быстроходных судов.
— Алюминиево-марганцевые сплавы во многом аналогичны алюминиево-магниевым.
— Алюминиево-медные сплавы (в частности, дюралюминий) можно подвергать термообработке, что намного повышает их прочность. К сожалению, термообработанные материалы нельзя сваривать, поэтому детали самолётов до сих пор соединяют заклёпками. Сплав с бо́льшим содержанием меди по цвету внешне очень похож на золото, и его иногда применяют для имитации последнего.
— Алюминиево-кремниевые сплавы (силумины) лучше всего подходят для литья. Из них часто отливают корпуса разных механизмов.
— Комплексные сплавы на основе алюминия: авиаль.
— Алюминий переходит в сверхпроводящее состояние при температуре 1,2 Кельвина.
Алюминий как добавка в другие сплавы
Алюминий является важным компонентом многих сплавов. Например, в алюминиевых бронзах основные компоненты — медь и алюминий. В магниевых сплавах в качестве добавки чаще всего используется алюминий. Для изготовления спиралей в электронагревательных приборах используют (наряду с другими сплавами) фехраль (Fe, Cr, Al).
Ювелирные изделия
Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Мода на них сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии.
Стекловарение
В стекловарении используются фторид, фосфат и оксид алюминия.
Пищевая промышленность
Алюминий зарегистрирован в качестве пищевой добавки Е173.
Алюминий и его соединения в ракетной технике
Алюминий и его соединения используются в качестве высокоэффективного ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах. Следующие соединения алюминия представляют наибольший практический интерес как ракетное горючее:
— Алюминий: горючее в ракетных топливах. Применяется в виде порошка и суспензий в углеводородах и др
— Гидрид алюминия
— Боранат алюминия
— Триметилалюминий
— Триэтилалюминий
— Трипропилалюминий
Теоретические характеристики топлив, образованных гидридом алюминия с различными окислителями.
| Окислитель | Удельная тяга (Р1, сек) | Температура сгорания °С | Плотность топлива, г/см³ | Прирост скорости, ΔVид, 25, м/с | Весовое содерж. горючего, % |
|---|---|---|---|---|---|
| Фтор | 348,4 | 5009 | 1,504 | 5328 | 25 |
| Тетрафторгидразин | 327,4 | 4758 | 1,193 | 4434 | 19 |
| ClF3 | 287,7 | 4402 | 1,764 | 4762 | 20 |
| ClF5 | 303,7 | 4604 | 1,691 | 4922 | 20 |
| Перхлорилфторид | 293,7 | 3788 | 1,589 | 4617 | 47 |
| Фторид кислорода | 326,5 | 4067 | 1,511 | 5004 | 38,5 |
| Кислород | 310,8 | 4028 | 1,312 | 4428 | 56 |
| Перекись водорода | 318,4 | 3561 | 1,466 | 4806 | 52 |
| N2O4 | 300,5 | 3906 | 1,467 | 4537 | 47 |
| Азотная кислота | 301,3 | 3720 | 1,496 | 4595 | 49 |
Алюминий в мировой культуре
Поэт Андрей Вознесенский написал в 1959 году стихотворение «Осень», в котором использовал алюминий в качестве художественного образа:
…А за окошком в юном инее
лежат поля из алюминия…
Виктор Цой написал песню «Алюминиевые огурцы» с припевом:
Сажаю алюминиевые огурцы
На брезентовом поле
Я сажаю алюминиевые огурцы
На брезентовом поле
Токсичность
Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. Наиболее ядовиты хлориды, нитраты, ацетаты, сульфаты и др. Для человека токсическое действие при попадании внутрь оказывают следующие дозы соединений алюминия (мг/кг массы тела): ацетат алюминия — 0,2-0,4; гидроксид алюминия — 3,7-7,3; алюминиевые квасцы — 2,9. В первую очередь действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). Однако свойство нейротоксичности алюминия стали изучать с середины 1960-х годов, так как накоплению металла в организме человека препятствует механизм его выведения. В обычных условиях с мочой может выделяться до 15 мг элемента в сутки. Соответственно, наибольший негативный эффект наблюдается у людей с нарушенной выделительной функцией почек.
Норматив содержания алюминия в воде хозяйственно-питьевого использования сотавляет 0,2 мг/л. При этом данная ПДК может быть увеличена до 0,5 мг/л главным государственным санитарным врачом по соответствующей территории для конкретной системы водоснабжения.
Дополнительная информация
— Гидроксид алюминия
— Энциклопедия об алюминии
— Соединения алюминия
— Международный институт алюминия
Вяжущие вещества, содержащие алюминий, известны с глубокой древности. Однако под квасцами (лат. Alumen или Alumin, нем. Alaun), о которых говорится, в частности, у Плиния, в древности и в средние века понимали различные вещества. В «Алхимическом словаре» Руланда слово Alumen с добавлением различных определений приводится в 34 значениях. В частности, оно означало антимоний, Alumen alafuri — алкалическую соль, Alumen Alcori — нитрум или алкалические квасцы, Alumen creptum — тартар (винный камень) хорошего вина, Alumen fascioli — щелочь, Alumen odig — нашатырь, Alumen scoriole — гипс и т. д. Лемери, автор известного «Словаря простых аптекарских товаров» (1716), также приводит большой перечень разновидностей квасцов.
До XVIII в. соединения алюминия (квасцы и окись) не умели отличать от других, похожих по внешнему виду соединений. Лемери следующим образом описывает квасцы: «В 1754 r. Маргграф выделил из раствора квасцов (действием щелочи) осадок окиси алюминия, названной им »квасцовой землей» (Alaunerde), и установил ее отличие от других земель. Вскоре квасцовая земля получила название алюмина (Alumina или Alumine). В 1782 г. Лавуазье высказал мысль, что алюмина представляет собой окисел неизвестного элемента. В «Таблице простых тел» Лавуазье поместил алюмину (Alumine) среди «простых тел, солеобразующих, землистых«. Здесь же приведены синонимы названия алюмина: аргила (Argile), квасцовая. земля, основание квасцов. Слово аргила, или аргилла, как указывает Лемери в своем словаре, происходит от греч. горшечная глина. Дальтон в своей »Новой системе химической философии» приводит специальный знак для алюмины и дает сложную структурную (!) формулу квасцов.
После открытия с помощью гальванического электричества щелочных металлов Дэви и Берцелиус безуспешно пытались выделить тем же путем металлический алюминий из глинозема. Лишь в 1825 г. задача была решена датским физиком Эрстедом химическим способом. Он пропускал хлор через раскаленную смесь глинозема с углем, и полученный безводный хлористый алюминий нагревал с амальгамой калия. После испарения ртути, пишет Эрстед, получался металл, похожий по внешнему виду на олово. Наконец, в 1827 г. Велер выделил металлический алюминий более эффективным способом — нагреванием безводного хлористого алюминия с металлическим калием.
Около 1807 г. Дэви, пытавшийся осуществить электролиз глинозема, дал название предполагаемому в нем металлу алюмиум (Alumium) или алюминум (Aluminum). Последнее название с тех пор ужилось в США, в то время как в Англии и других странах принято предложенное впоследствии тем же Дэви название алюминиум (Aluminium). Вполне ясно, что все эти названия произошли от латинского слова квасцы (Alumen), насчет происхождения которого существуют разные мнения, базирующиеся на свидетельствах различных авторов, начиная с древности.
А. М. Васильев, отмечая неясное происхождение этого слова, приводит мнение некоего Исидора (очевидно Исидора Севильского, епископа, жившего в 560 — 636 гг.,- энциклопедиста, занимавшегося, в частности, этимологическими исследованиями): «Alumen называют a lumen, так как он придает краскам lumen (свет, яркость), будучи добавлен при крашении«. Однако это, хотя и очень давнее, объяснение не доказывает, что слово alumen имеет именно такие истоки. Здесь вполне вероятна лишь случайная тавтология. Лемери (1716) в свою очередь указывает, что слово alumen связано с греческим (халми), означающим соленость, соляной раствор, рассол и пр.
Русские названия алюминия в первые десятилетия XIX в. довольно разнообразны. Каждый из авторов книг по химии этого периода, очевидно, стремился предложить свое название. Так, Захаров именует алюминий глиноземом (1810), Гизе — алумием (1813), Страхов — квасцом (1825), Иовский — глинистостью, Щеглов — глиноземием (1830). В »Магазине Двигубского» (1822 — 1830) глинозем называется алюмин, алюмина, алумин (например, фосфорно-кисловатая алюмина), а металл — алуминий и алюминий (1824). Гесс в первом издании «Оснований чистой химии» (1831) употребляет название глиноземий (Aluminium), а в пятом издании (1840) — глиний. Однако названия для солей он образует на основе термина глинозем, например сернокислый глинозем. Менделеев в первом издании »Основ химии” (1871) пользуется названиями алюминий и глиний. В дальнейших изданиях слово глиний уже не встречается.
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 | 1 H Водород |
2 He Гелий |
||||||||||||||||
| 2 | 3 Li Литий |
4 Be Бериллий |
5 B Бор |
6 C Углерод |
7 N Азот |
8 O Кислород |
9 F Фтор |
10 Ne Неон |
||||||||||
| 3 | 11 Na Натрий |
12 Mg Магний |
13 Al Алюминий |
14 Si Кремний |
15 P Фосфор |
16 S Сера |
17 Cl Хлор |
18 Ar Аргон |
||||||||||
| 4 | 19 K Калий |
20 Ca Кальций |
21 Sc Скандий |
22 Ti Титан |
23 V Ванадий |
24 Cr Хром |
25 Mn Марганец |
26 Fe Железо |
27 Co Кобальт |
28 Ni Никель |
29 Cu Медь |
30 Zn Цинк |
31 Ga Галлий |
32 Ge Германий |
33 As Мышьяк |
34 Se Селен |
35 Br Бром |
36 Kr Криптон |
| 5 | 37 Rb Рубидий |
38 Sr Стронций |
39 Y Иттрий |
40 Zr Цирконий |
41 Nb Ниобий |
42 Mo Молибден |
(43) Tc Технеций |
44 Ru Рутений |
45 Rh Родий |
46 Pd Палладий |
47 Ag Серебро |
48 Cd Кадмий |
49 In Индий |
50 Sn Олово |
51 Sb Сурьма |
52 Te Теллур |
53 I Иод |
54 Xe Ксенон |
| 6 | 55 Cs Цезий |
56 Ba Барий |
* | 72 Hf Гафний |
73 Ta Тантал |
74 W Вольфрам |
75 Re Рений |
76 Os Осмий |
77 Ir Иридий |
78 Pt Платина |
79 Au Золото |
80 Hg Ртуть |
81 Tl Таллий |
82 Pb Свинец |
83 Bi Висмут |
(84) Po Полоний |
(85) At Астат |
86 Rn Радон |
| 7 | 87 Fr Франций |
88 Ra Радий |
** | (104) Rf Резерфордий |
(105) Db Дубний |
(106) Sg Сиборгий |
(107) Bh Борий |
(108) Hs Хассий |
(109) Mt Мейтнерий |
(110) Ds Дармштадтий |
(111) Rg Рентгений |
(112) Cp Коперниций |
(113) Uut Унунтрий |
(114) Uuq Унунквадий |
(115) Uup Унунпентий |
(116) Uuh Унунгексий |
(117) Uus Унунсептий |
(118) Uuo Унуноктий |
| 8 | (119) Uue Унуненний |
(120) Ubn Унбинилий |
||||||||||||||||
| Лантаноиды * | 57 La Лантан |
58 Ce Церий |
59 Pr Празеодим |
60 Nd Неодим |
(61) Pm Прометий |
62 Sm Самарий |
63 Eu Европий |
64 Gd Гадолиний |
65 Tb Тербий |
66 Dy Диспрозий |
67 Ho Гольмй |
68 Er Эрбий |
69 Tm Тулий |
70 Yb Иттербий |
71 Lu Лютеций |
|||
| Актиноиды ** | 89 Ac Актиний |
90 Th Торий |
91 Pa Протактиний |
92 U Уран |
(93) Np Нептуний |
(94) Pu Плутоний |
(95) Am Америций |
(96) Cm Кюрий |
(97) Bk Берклий |
(98) Cf Калифорний |
(99) Es Эйнштейний |
(100) Fm Фермий |
(101) Md Менделевий |
(102) No Нобелей |
(103) Lr Лоуренсий |
|||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
198095, г.Санкт-Петербург, ул.Швецова, д.23, лит.Б, пом.7-Н, схема проезда
Источник статьи: http://himsnab-spb.ru/article/ps/al/